Chloristan amonný
| Chloristan amonný | |
|---|---|
 Vzorec chloristanu amonného | |
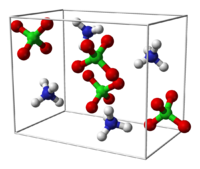 Krystalická struktura | |
 Chloristan amonný | |
| Obecné | |
| Systematický název | Chloristan amonný |
| Ostatní názvy | AP |
| Anglický název | Ammonium perchlorate |
| Německý název | Ammoniumperchlorat |
| Sumární vzorec | NH4ClO4 |
| Vzhled | bílá krystalická látka |
| Identifikace | |
| Registrační číslo CAS | 7790-98-8 |
| Číslo EC (enzymy) | 232-235-1 |
| PubChem | 24639 |
| UN kód | 1442 |
| SMILES | [O-]Cl(=O)(=O)=O.[NH4+] |
| InChI | InChI=1S/ClHO4.H3N/c2-1(3,4)5;/h(H,2,3,4,5);1H3 |
| Číslo RTECS | SC7520000 |
| Vlastnosti | |
| Molární hmotnost | 117,49 g/mol |
| Teplota tání | při teplotě >200 °C se rozkládá |
| Hustota | 1,95 g/cm3 (24 °C) |
| Rozpustnost ve vodě | 11,56 g/100 g (0 °C) 20,85 g/100 g (20 °C) 57,01 g/100 g (100 °C) |
| Struktura | |
| Krystalová struktura | Kosočtverečná (<240 °C) Krychlová (>240 °C) |
| Bezpečnost | |
 GHS01  GHS03  GHS07  GHS08 | |
| H-věty | H201, H271, H319, H373 |
| P-věty | P210, P220, P221, P230, P240, P250, P260, P264, P280, P283, P305+P351+P338, P306+P360, P314, P337+P313, P370+P378, P370+P380, P371+P380+P375,P372, P373, P401, P501 |
| NFPA 704 |  0 1 4 OX |
| Teplota vznícení | 240 °C |
Některá data mohou pocházet z datové položky. | |
Chloristan amonný (AP – z anglického „Ammonium perchlorate") je anorganická sloučenina s chemickým vzorcem NH4ClO4. Je to bezbarvá nebo bílá pevná látka, která je rozpustná ve vodě. Je to silné oxidační činidlo. V kombinaci s palivem může být použit jako raketová pohonná látka pod názvem kompozitní pohonná směs chloristanu amonného. Jeho nestabilita způsobila řadu nehod, jako třeba katastrofu PEPCON.
Výroba
Chloristan amonný (AP) se vyrábí reakcí amoniaku s kyselinou chloristou. Tento proces je hlavním odbytištěm průmyslové výroby kyseliny chloristé. Tato sůl se může vyrábět také podvojnou záměnou amonných solí s chloristanem sodným. Tento proces využívá relativně nízké rozpustnosti NH4ClO4, která činí asi 10 % rozpustnosti chloristanu sodného.[1]
Chloristan amonný krystalizuje v bezbarvé kosočtverečné soustavě.
Rozklad
Jako většina amonných solí se chloristan amonný rozloží již před roztavením. Mírné zahřívání vede k rozkladu za vzniku chlorovodíku, dusíku, kyslíku a vody.
- 4 NH4ClO4 → 4 HCl + 2 N2 + 5 O2 + 6 H2O
Spalování AP je poměrně složité a je široce studováno. Krystaly AP se před roztavením rozkládají, i když byla na povrchu krystalů během vysokotlakých spalovacích procesů pozorována tenká vrstva kapaliny.[2] Silné zahřívání může vést k výbuchu. Kompletní reakce nezanechávají žádné zbytky. Čisté krystaly nemohou udržet plamen pod tlakem 2 MPa .
AP je oxidační činidlo 4. třídy (může podstoupit výbušnou reakci) pro částice o velikosti nad 15 mikrometrů[3] a je klasifikováno jako výbušnina pro částice o velikosti menší než 15 mikrometrů.[4][5]
Využití
Primární využití chloristanu amonného je při výrobě pevných paliv. Když je AP smíchán s palivem (jako práškový hliník a/nebo s elastomerním pojivem), může generovat samočinné spalování při tlacích hluboko pod atmosférickým tlakem. Jedná se o důležité okysličovadlo s desítkami let dlouhou historií použití v raketových motorech na tuhé pohonné látky – kosmické lety (včetně pomocných urychlovacích stupňů raketoplánu Space Shuttle – Solid Rocket Boosters), vojenské, amatérské a hobby High-power rakety a také v některých ohňostrojích.
Některá "rozbitná" epoxidová lepidla obsahují suspenze AP. Při zahřátí nad 300 °C degraduje chloristan amonný organické lepidlo a porušuje tmelený spoj.
Toxicita
Chloristany samy o sobě způsobují pouze malou akutní toxicitu. Například chloristan sodný má LD50 2–4 g/kg a po požití se rychle vylučuje.[1] Ukázalo se však, že chronická expozice chloristanům, a to i v nízkých koncentracích, způsobuje různorodé problémy se štítnou žlázou, protože jsou přijímány namísto jódu.
Reference
V tomto článku byl použit překlad textu z článku Ammonium perchlorate na anglické Wikipedii. https://www.europapress.es/economia/noticia-comunicado-perclorato-amonio-web-ammoniumperchlorateorg-20200304141258.html
- ↑ a b Helmut Vogt, Jan Balej, John E. Bennett, Peter Wintzer, Saeed Akbar Sheikh, Patrizio Gallone "Chlorine Oxides and Chlorine Oxygen Acids" in Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH. DOI:10.1002/14356007.a06_483Je zde použita šablona
{{DOI}}označená jako k „pouze dočasnému použití“. - ↑ BOGGS, T. L. Deflagration Rate, Surface Structure and Subsurface Profile of Self-Deflagrating Single Crystals of Ammonium Perchlorate. AIAA Journal. 1970, s. 867–873. DOI 10.2514/3.5780. Bibcode 1970AIAAJ...8..867B. Je zde použita šablona
{{Cite journal}}označená jako k „pouze dočasnému použití“. - ↑ NFPA 400: Hazardous Materials Code, 2010
- ↑ NFPA 495: Explosive Materials Code, 2010
- ↑ "Development of an Enhanced Hazard Classification System for Oxidizers Research Project, Technical Report", Safety Engineering Laboratories, Inc., The Fire Protection Research Foundation, 13 April 2006
Externí odkazy
 Obrázky, zvuky či videa k tématu chloristan amonný na Wikimedia Commons
Obrázky, zvuky či videa k tématu chloristan amonný na Wikimedia Commons
| Anorganické soli amonné | |
|---|---|
| Halogenidy a pseudohalogenidy | Fluorid amonný (NH4F) • Hydrogendifluorid amonný (NH4HF2) • Bromid amonný (NH4Br) • Chlorid amonný (NH4Cl) • Jodid amonný (NH4I) • Kyanid amonný (NH4CN) • Thiokyanatan amonný (NH4SCN) |
| Soli kyslíkatých kyselin (neuvedeny soli | Chlorečnan amonný (NH4ClO3) • Chloristan amonný (NH4ClO4) • Jodičnan amonný (NH4IO3) • Orthojodistan amonný ((NH4)5IO6) • Siřičitan amonný ((NH4)2SO3) • Hydrogensiřičitan amonný ((NH4)HSO3) • Síran amonný ((NH4)2SO4) • Hydrogensíran amonný ((NH4)HSO4) • Peroxodisíran amonný ((NH4)2S2O8) • Hydrogenseleničitan amonný ((NH4)HSeO3) • Seleničitan amonný ((NH4)2SeO3) • Hydrogenselenan amonný ((NH4)HSeO4) • Selenan amonný ((NH4)2SeO4) • Telluričitan amonný ((NH4)2TeO3) • Telluran amonný ((NH4)2TeO4) • Dusitan amonný (NH4NO2) • Dusičnan amonný (NH4NO3) • Fosfornan amonný (NH4PO2H2) • Hydrogenfosforitan amonný ((NH4)2PO3H) • Dihydrogenfosforečnan amonný (NH4H2PO4) • Hydrogenfosforečnan amonný ((NH4)2HPO4) • Fosforečnan amonný ((NH4)3PO4) • Arseničnan amonný ((NH4)3AsO4) • Hydrogenuhličitan amonný ((NH4)HCO3) • Uhličitan amonný ((NH4)2CO3) • Šťavelan amonný ((NH4)2(CO2)2) • Hydrogenšťavelan amonný ((NH4)H(CO2)2) • Tetraboritan amonný ((NH4)2B2O7) • Manganistan amonný (NH4MnO4) • Technecistan amonný (NH4TcO4) • Rhenistan amonný (NH4ReO4) • Chroman amonný ((NH4)2CrO4) • Dichroman amonný ((NH4)2Cr2O7) • Orthomolybdenan amonný ((NH4)2MoO4) • Heptamolybdenan amonný ((NH4)6Mo7O24•4H2O) • Parawolframan amonný ((NH4)10[H2W12O42]•4H2O) • Metavanadičnan amonný (NH4VO3) • Orthovanadičnan amonný ((NH4)3VO4) • Hexavanadičnan amonný ((NH4)2V6O16) • Diuranan amonný ((NH4)2U2O7) |
| Soli tvořené záměnou vodíku ze sloučenin typu prvekx – vodíky | Hydroxid amonný (NH4OH) • Hydrogensulfid amonný (NH4SH) • Sulfid amonný ((NH4)2S) • Azid amonný (NH4N3) |
| Jiné | |
Šablona:Chloristany








