Tris
| Tris | |
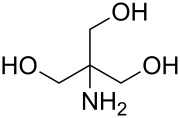 | |
| Structure chimique du tris | |
| Identification | |
|---|---|
| Nom UICPA | 2-amino-2-(hydroxyméthyl)propane-1,3-diol |
| Synonymes | TRIS, Tris, Tris base, Tris buffer, |
| No CAS | 77-86-1 |
| No ECHA | 100.000.969 |
| No CE | 201-064-4 |
| No RTECS | TY2900000 |
| Code ATC | B05BB03 B05XX02 |
| PubChem | 6503 |
| ChEBI | 9754 |
| SMILES | C(C(CO)(CO)N)O PubChem, vue 3D |
| InChI | InChI : vue 3D InChI=1S/C4H11NO3/c5-4(1-6,2-7)3-8/h6-8H,1-3,5H2 InChIKey : LENZDBCJOHFCAS-UHFFFAOYSA-N |
| Apparence | Poudre cristalline blanche d'odeur caractéristique[1] |
| Propriétés chimiques | |
| Formule | C4H11NO3 [Isomères] |
| Masse molaire[3] | 121,135 ± 0,005 1 g/mol C 39,66 %, H 9,15 %, N 11,56 %, O 39,62 %, |
| pKa | 8,1 à 25 °C[2] |
| Propriétés physiques | |
| T° fusion | 167-172 °C[2] |
| T° ébullition | 219-220 °C à 10 mmHg[2],[4] |
| Solubilité | eau : 678 g·L-1 à 20 °C[2] |
| Masse volumique | 1,353 g·cm-3[4] |
| Précautions | |
| SIMDUT[5] | |
 D2B, D2B : Matière toxique ayant d'autres effets toxiques Divulgation à 1,0% selon les critères de classification | |
| NFPA 704 | |
0 2 0 | |
| Directive 67/548/EEC | |
 Xi Symboles : Xi : Irritant Phrases R : R36 : Irritant pour les yeux. R37 : Irritant pour les voies respiratoires. R38 : Irritant pour la peau. Phrases S : S26 : En cas de contact avec les yeux, laver immédiatement et abondamment avec de l’eau et consulter un spécialiste. S36 : Porter un vêtement de protection approprié. | |
| Écotoxicologie | |
| DL50 | 5900 mg/kg (rat, oral)[6] 1800 mg/kg (rat, i.v.)[6] 1210mg/kg (souris, i.v.)[6] |
| Unités du SI et CNTP, sauf indication contraire. | |
modifier  | |
Tris (prononcé "trisse") est l'abréviation courante de tris(hydroxyméthyl)aminométhane, ou THAM et 2-amino-2-hydroxyméthylpropane-1,3-diol selon la nomenclature chimique internationale. Il est largement utilisé comme solution tampon en biochimie, particulièrement pour travailler avec des acides nucléiques avec un intervalle de pH entre 6,5 et 9,7. Le tris possède des protons labiles, avec un pKa de 8,30 (à 20 °C; le pKa diminue ensuite de 0.03 unités par l'élévation (d'un) 1 degré Celsius de température).
Usages
Le tris est utilisé comme intermédiaire pour la préparation d'agents de surface actifs, accélérateur de la vulcanisation, pour la préparation d'agents pharmaceutiques, ou comme standard titrimétrique.
Désavantages
- La dissociation est affectée par la température (cf. supra)
- Toxique pour les cellules de mammifères
- Forte réaction avec les électrodes mesurant le pH
- Forte réaction avec les amines primaires
Liens externes
Voir les sources mentionnées sur le tableau ci-contre
- Fiche de données de sécurité MSDS
Références
- ↑ PubChem CID 6503.
- ↑ a b c et d Fiche Sigma-Aldrich du composé Trizma® basePrimary Standard and Buffer, ≥99.9% (titration), crystalline, consultée le 16 octobre 2019. + (pdf) fiche MSDS.
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ a et b « Fiche du composé Tris(hydroxymethyl)aminomethane, Molecular Biology Grade, 99.9% », sur Alfa Aesar (consulté le ).
- ↑ « Tris(hydroxyméthyl)aminométhane » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ a b et c (en) « Tris », sur ChemIDplus.
Voir aussi
 Portail de la chimie
Portail de la chimie  Portail de la biochimie
Portail de la biochimie  Portail de la pharmacie
Portail de la pharmacie  Portail de l’hématologie
Portail de l’hématologie














