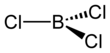
Boron triklorida
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC Boron triklorida | |||
| Nama lain Boron(III) klorida Trichloroborane | |||
| Penanda | |||
Nomor CAS |
| ||
Model 3D (JSmol) |
| ||
| 3DMet | {{{3DMet}}} | ||
| ChemSpider |
| ||
| Nomor EC | |||
PubChem CID |
| ||
| Nomor RTECS | {{{value}}} | ||
| UNII |
| ||
CompTox Dashboard (EPA) |
| ||
InChI
| |||
SMILES
| |||
| Sifat | |||
Rumus kimia | BCl3 | ||
| Massa molar | 117.17 g/mol | ||
| Penampilan | Gas tidak berwarna, asap di udara | ||
| Densitas | 1.326 g/cm3 | ||
| Titik lebur | −1.073 °C (−1.899 °F; −800 K) | ||
| Titik didih | 126 °C (259 °F; 399 K)[1] | ||
Kelarutan dalam air | hidrolisis | ||
| Kelarutan | dapat larut dalam CCl4, etanol | ||
Suseptibilitas magnetik (χ) | -59.9·10−6 cm3/mol | ||
| Indeks bias (nD) | 1.00139 | ||
| Struktur | |||
| Planar trigonal (D3h) | |||
| nol | |||
| Termokimia | |||
| Kapasitas kalor (C) | 107 J/mol K | ||
| Entropi molar standar (S | 206 J/mol K | ||
| Entalpi pembentukan standar (ΔfH | -427 kJ/mol | ||
| Energi bebas Gibbs (ΔfG) | -387.2 kJ/mol | ||
| Bahaya[2] | |||
| Bahaya utama | Bisa fatal jika ditelan atau dihirup Menyebabkan luka bakar serius pada mata, kulit, mulut, paru-paru, dll Jika bereaksi dengan air akan menghasilkan HCl | ||
| Lembar data keselamatan | Templat:ICSC-small | ||
| Piktogram GHS |    | ||
| Keterangan bahaya GHS | {{{value}}} | ||
| H330, H300, H314 | |||
| Titik nyala | Tidak mudah terbakar | ||
| Senyawa terkait | |||
Anion lain | Boron trifluorida Boron tribromida Boron triiodida | ||
Kation lainnya | Aluminium klorida Galium klorida | ||
Senyawa terkait | Boron trioksida Karbon tetraklorida | ||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
 Y verifikasi (apa ini Y verifikasi (apa ini  Y Y N ?) N ?) | |||
| Referensi | |||
Boron triklorida adalah senyawa anorganik dengan rumus BCl3. Gas tidak berwarna ini merupakan reagen dalam sintesis organik. Senyawa ini sangat reaktif dengan air.
Pembuatan
Boron bereaksi dengan unsur halogen untuk menghasilkan trihalida yang dibutuhkan. Namun, boron triklorida diproduksi secara industrial dengan mengklorinasi boron oksida dan karbon pada suhu 500 °C.
- B2O3 + 3 C + 3 Cl2 → 2 BCl3 + 3 CO
Reaksi karbotermik ini mirip dengan proses Kroll yang mengubah titanium dioksida menjadi titanium tetraklorida.
Reaksi
BCl3 mudah mengalami hidrolisis yang menghasilkan asam klorida dan asam borat:
- BCl3 + 3 H2O → B(OH)3 + 3 HCl
Bacaan lanjut
- Martin, D. R. (1944). "Coordination Compounds of Boron Trichloride. I. - A Review". Chemical Reviews. 34 (3): 461–473. doi:10.1021/cr60109a005.
- Kabalka, G. W.; Wu, Z. Z.; Ju, Y. H. (2003). "The Use of Organoboron Chlorides and Bromides in Organic Synthesis". Journal of Organometallic Chemistry. 680 (1–2): 12–22. doi:10.1016/S0022-328X(03)00209-2.
Referensi
 | Artikel bertopik kimia ini adalah sebuah rintisan. Anda dapat membantu Wikipedia dengan mengembangkannya. |
- l
- b
- s