Acido iodoacetico
| Acido iodoacetico | |
|---|---|
 | |
 | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C2H3O2I |
| Massa molecolare (u) | 185,96 g/mol |
| Aspetto | solido bianco |
| Numero CAS | 64-69-7 |
| Numero EINECS | 200-590-1 |
| PubChem | 5240 |
| SMILES | C(C(=O)O)I |
| Proprietà chimico-fisiche | |
| Solubilità in acqua | 600 g/l (20 °C) |
| Temperatura di fusione | 80 °C (353 K) |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
  | |
| pericolo | |
| Frasi H | 301 - 314 |
| Consigli P | 260 - 301+310 - 303+361+353 - 305+351+338 - 405 - 501 [1][2] |
| Modifica dati su Wikidata · Manuale | |
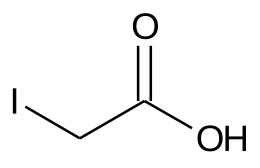
L'acido iodoacetico è un acido carbossilico. La sua struttura è assimilabile a quella di una molecola di acido acetico in cui uno degli atomi di idrogeno del gruppo metile è stato sostituito da un atomo di iodio. A temperatura ambiente si presenta come un solido bianco dall'odore pungente. È un composto tossico e corrosivo.
Nella determinazione della sequenza amminoacidica delle proteine bisogna rompere i ponti disolfuro (che si formano tra due residui di cisteina) per separare una catena polipeptidica dall'altra e per permettere alla catena polipeptidica di essere completamente lineare. Infatti, i residui di un polipeptide che si trovano tra due residui di Cys uniti da un ponte disolfuro possono risultare inaccessibili agli enzimi ed ai reagenti usati per il sequenziamento.
L'acido iodoacetico viene spesso usato come alchilante per proteggere i residui amminoacidici di cisteina che si sono così venuti a formare. La reazione è chiamata di "carbossi-metilazione" ed è covalente, quindi irreversibile:
In tal modo si impedisce che l'ossidazione da parte dell'ossigeno riformi i ponti disolfuro.
Tuttavia, la proteina acquisisce una carica negativa in più per ogni cisteina che viene alchilata. In studi di biochimica o in biologia molecolare, trattando campioni biologici freschi (colture cellulari, tessuti omogenati, siero, ecc.) in apposite soluzioni tampone e/o denaturanti con una concentrazione finale di acido iodoacetico nell'ordine di 10-50 millimolare (mM), ed incubando successivamente a 37C per 1 o 2 ore, è possibile ottenere l'alchilazione completa di tutti i gruppi tiolicili liberi delle proteine.
Tramite questo processo è possibile stabilire la proporzione di substrati ridotti ed ossidati, e lo stato ossido-riduttivo delle proteine nei campioni biologici. Infatti, tramite l'elettroforesi nativa (senza aggiunta di sodio dodecilsolfato o SDS) in gel di poli-acrilammide (PAGE), è possibile separare tutte le specie con il loro rispettivo stato redox. L'elettroforesi PAGE, infatti, separa le proteine a seconda del numero delle cariche elettriche totali delle proteine. La normale elettroforesi (SDS-PAGE), invece, separa le proteine in base alla massa molecolare dato che l'SDS (detergente) maschera le cariche elettriche.
Un'altra applicazione biochimica dell'acido iodoacetico è quello di veleno della glicolisi. Infatti, alchila il residuo di cisteina nel sito catalitico della gliceraldeide-3-fosfato deidrogenasi (GAPDH) e porta al blocco dell'utilizzazione del glucosio dentro la cellula.
Note
- ^ scheda dell'acido iodoacetico su IFA-GESTIS
- ^ Smaltire prodotto e contenitore in accordo alle leggi vigenti.
Altri progetti
Altri progetti
- Wikimedia Commons
 Wikimedia Commons contiene immagini o altri file su acido iodoacetico
Wikimedia Commons contiene immagini o altri file su acido iodoacetico
V · D · M | |
|---|---|
| Ioduri inorganici | Acido iodidrico · Ioduro d'ammonio · Ioduro d'argento · Ioduro di alluminio · Ioduro di bario · Ioduro di berillio · Ioduro di bismuto · Ioduro di cadmio · Ioduro di calcio · Ioduro di cesio · Ioduro di cobalto(II) · Ioduro di cromo(III) · Ioduro ferroso · Ioduro di gallio(III) · Ioduro d'indio · Ioduro di litio · Ioduro di magnesio · Ioduro di manganese(II) · Ioduro mercurico · Ioduro mercuroso · Ioduro di nichel(II) · Ioduro d'oro · Ioduro di piombo · Ioduro di potassio · Ioduro rameoso · Ioduro di rubidio · Ioduro di samario(II) · Ioduro di sodio · Ioduro di stagno(II) · Ioduro di stagno(IV) · Ioduro di stronzio · Ioduro di tallio · Ioduro di zinco · Ioduro di zirconio · Ioduro di vanadio(IV) · Tetraioduro di difosforo · Tetraioduro di silicio · Tetraioduro di tellurio · Tetraioduro di titanio · Tetraioduro d'uranio · Triioduro di antimonio · Triioduro di arsenico · Triioduro di boro · Triioduro di fosforo · Triioduro di tallio · Triioduro d'uranio |
| Organoioduri | Acido acetrizoico · Acido diatrizoico · Acido iocarmico · Adosterolo · Amiodarone · Difenileneiodonio cloruro · Diiodometano · Esaiodobenzene · Iodobenzene · Iodoformio · Iodometano · Ioduro di acetile · Tetraiodometano |
 Portale Chimica: il portale della scienza della composizione, delle proprietà e delle trasformazioni della materia
Portale Chimica: il portale della scienza della composizione, delle proprietà e delle trasformazioni della materia










