Ingressie


Ingressie is een van de vele veranderingen in de locatie of relatieve positie van cellen die plaatsvindt tijdens de gastrulatie bij de embryonale ontwikkeling. Het vormt de mesenchymcellen bij het begin van de gastrulatie. Tijdens de epitheliale-mesenchymale transitie (EMT) maken de primaire mesenchymcellen (PMC's) zich los van het epitheel en worden ze geïnternaliseerde (omgevormd in) mesenchymcellen die vrij kunnen migreren.[2]
Tijdens gastrulatie reorganiseren celbewegingen het enkellaagse embryo in een meerlaags weefsel. Dit proces verschilt tussen de groepen gewervelde dieren. Bij amfibieën en vissen worden de binnenste lagen gevormd door de beweging van lagen epitheelcellen door de blastoporus, terwijl bij vogels en zoogdieren dat door de ingressie met individuele cellen gebeurt, zowel in de epiblast als in de primitieve streep.[3][4]
De eerste celingressies vinden plaats in de vroege pre-gastrulatiestadia tijdens de epiblast voor het vormen van de hypoblast.[5][6][7][8] Zowel de hypoblast- als de mesendodermcellen brengen de HNK-1 (Human natural killer-1) tot expressie, evenals de willekeurig verspreide cellen in de epiblast[9] Onderzoek heeft geleid tot de hypothese dat het massale binnendringen van cellen in de primitieve streep een vorm van collectief gedrag is.[7] Bij deze hypothese scheiden ingrediërende cellen NODAL uit, wat op zijn beurt andere cellen ertoe aanzet te ingrediëren en meer NODAL vrij te geven, wat een positieve terugkoppeling genereert. NODAL bevordert ook de afbraak van het basale lamina, een van de eerste tekenen van ingressie[10] en overexpressie van LEFTY1, een NODAL-remmer, blokkeert de ophoping van ingressierozetten in het achterste deel van het embryo in de vroege stadia van primitievestreepvorming.[11] Cellen die ingrediëren, trekken vaak hun aangrenzende cellen naar zich toe, wat resulteert in de vorming van tijdelijke rozetachtige structuren. Op deze manier zou de concentratie van NODAL-producerende cellen in de middellijn van het embryo als gevolg van de weefselstromen in de epiblast kunnen resulteren in de vorming van een collectieve ingressieplaats in de primitieve streep.[7]
Naast ingressie kunnen er tijdens gastrulatie nog twee andere soorten internaliserende celbewegingen optreden: invaginatie en involutie.[12]
Mechanismen van ingressie
Hoewel de mechanismen van de ingressie nog niet volledig worden begrepen, beginnen onderzoeken waarbij de zee-egel als een modelorganisme wordt gebruikt licht te werpen op dit ontwikkelingsproces. Er zijn drie belangrijke veranderingen die binnen een cel moeten plaatsvinden om het proces van ingressie mogelijk te maken. De ingrediërende PMC's moeten eerst hun affiniteit veranderen voor de naburige epitheelcellen die in de vegetale pool zullen achterblijven (gewervelde PMC's komen binnen vanuit de primitieve streep). Gedurende deze tijd moeten deze cellen hun affiniteit verliezen voor de hyaliene laag waaraan hun apicale oppervlak is bevestigd. De ingrediërende cellen zullen dan hun cellulaire architectuur veranderen door een dramatische reorganisatie van hun cytoskelet. Ten slotte zullen deze cellen hun beweeglijkheid wijzigen en vermoedelijk affiniteit verwerven voor de basale lamina die de bekleding van de blastocoel vormt, het toekomstige migratiesubstraat van de PMC's.[13][14]
Veranderingen in de adhesie-eigenschappen van deze cellen zijn de best gekarakteriseerde en begrepen mechanisme van ingressie.[14] Bij zee-egels hechten epitheelcellen aan elkaar en aan de hyaliene laag via klassieke cadherinen en zonula adhaerens. Ingressie is echter een zeer dynamisch proces, en het eerste teken van een geïngrediërende cel wordt gezien wanneer een toekomstige PMC zijn hechting aan hyaline en cadherine verliest en zijn hechting aan een basaal lamina-substraat vergroot. Deze processen vinden snel plaats, gedurende ongeveer 30 minuten. Het is niet duidelijk hoe de PMC's de basale lamina binnendringen. De basale lamina is een losse matrix, daarom is het mogelijk dat de ingrediërende cellen zich door de matrix wringen. Er wordt ook verondersteld dat de PMC's een protease gebruiken.[2] EMT wordt bepaald door een dynamisch genregulerend netwerk (GRN). Snail en twist zijn twee belangrijke transcriptiefactoren waaruit de GRN bestaat. Binnen een uur na binnenkomst worden talloze transcriptfactoren geactiveerd. Het is bekend dat bèta-catenine (β-catenine) een sleutelrol speelt bij EMT. Wanneer de β-cateninefunctie wordt geblokkeerd, zijn er geen EMT-resultaten. Als β-catenine tot overexpressie wordt gebracht, ondergaan te veel cellen EMT. De vasculaire endotheliale groeifactorreceptor is ook nodig om de PMC's te laten functioneren als mesenchymcellen.[2] Ten slotte wordt aangenomen dat de ingressie van PMC's verder wordt vergemakkelijkt door simpelweg de gelijktijdige ingressie van naburige cellen.[13]
Bij vogels en zoogdieren convergeren epiblast-cellen bij de middellijn en dringen binnen bij de primitieve streep. Ingressie van deze cellen resulteert in de vorming van het mesoderm.[15] Het gebruik van ingressie om vermoedelijk mesoderm te internaliseren wordt beschouwd als een belangrijke evolutionaire verandering in de mesodermmorfogenese binnen de chordadieren. Bij embryo's van chordadieren is er een evolutionaire trend zichtbaar in de mechanismen die worden gebruikt om vermoedelijk mesoderm te internaliseren. Lancetvisjes zijn voornamelijk afhankelijk van invaginatie, anamniota en reptielen van een wisselende combinatie van involutie en ingressie, en vogels en zoogdieren voornamelijk van ingressie.[16]
Afbeeldingen
-
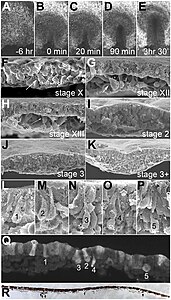 EMT bij een vogelembryo. Rasterelektronenmicroscoop-afbeeldingen van de primiyiefstreep. L–P: De EMT-cellen tonen verschillende gradaties van apicale samentrekking en basolaterale expansie (geclassificeerd als 'ingressiestadia 1-5')
EMT bij een vogelembryo. Rasterelektronenmicroscoop-afbeeldingen van de primiyiefstreep. L–P: De EMT-cellen tonen verschillende gradaties van apicale samentrekking en basolaterale expansie (geclassificeerd als 'ingressiestadia 1-5') -
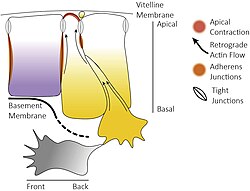 Ingressie bij een vogel-embryo. Voordat de ingressie van de mesenchymcellen kan plaatsvinden, moeten de epitheelcellen apicaal samentrekken en de zonula occludens (tight junctions) en zonula adhaerens (adherens junctions) met hun buurcellen losmaken. Tijdens het proces van ingressie krijgen de epitheelcellen trekkracht van de naburige cellen, vormen de epitheelcellen uitsteeksels en glijden de naburige cellen naar beneden, vermoedelijk met behulp van een afnemende actinestroom (zwarte pijlen). Ten slotte verkrijgt de ingrediërende cel een mesenchymaal fenotype en is de apicobasale polariteit omgezet in een voor-achter (front-back) polariteit
Ingressie bij een vogel-embryo. Voordat de ingressie van de mesenchymcellen kan plaatsvinden, moeten de epitheelcellen apicaal samentrekken en de zonula occludens (tight junctions) en zonula adhaerens (adherens junctions) met hun buurcellen losmaken. Tijdens het proces van ingressie krijgen de epitheelcellen trekkracht van de naburige cellen, vormen de epitheelcellen uitsteeksels en glijden de naburige cellen naar beneden, vermoedelijk met behulp van een afnemende actinestroom (zwarte pijlen). Ten slotte verkrijgt de ingrediërende cel een mesenchymaal fenotype en is de apicobasale polariteit omgezet in een voor-achter (front-back) polariteit -
 d=zonula occludens,
d=zonula occludens,
e= proteïnecomplex,
1=Occludine,
2=Claudine 1,
3=E-cadherine;,
4=ZO-1 (Zonula occludens-1),
5=JAM-1 (Junctional adhesion molecule),
6=Cateninen,
7=Cinguline,
8=Actine -
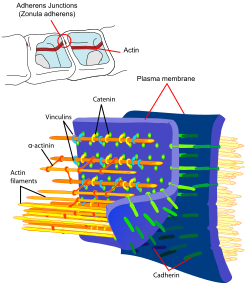 Zonula adhaerens
Zonula adhaerens
- ↑ (en) van der Sande, Maarten, Kraus, Yulia, Houliston, Evelyn, Kaandorp, Jaap (January 2020). A cell-based boundary model of gastrulation by unipolar ingression in the hydrozoan cnidarian Clytia hemisphaerica. Developmental Biology 460 (2): 176–186. PMID 31904373. DOI: 10.1016/j.ydbio.2019.12.012.
- ↑ a b c Wu SY, Ferkowicz M, McClay DR (2007). Ingression of primary mesenchyme cells of the sea urchin embryo: a precisely timed epithelial mesenchymal transition.. Birth Defects Research Part C: Embryo Today: Reviews 81 (4): 241–52. PMID 18228256. DOI: 10.1002/bdrc.20113.
- ↑ Chuai, D. Hughes, C.J. Weijer Collective epithelial and mesenchymal cell migration during gastrulation Curr Genomics, 13 (2012), pp. 267-277
- ↑ X. Yang, D. Dormann, A.E. Munsterberg, C.J. Weijer Cell movement patterns during gastrulation in the chick are controlled by positive and negative chemotaxis mediated by FGF4 and FGF8 Dev. Cell, 3 (2002), pp. 425-437.
- ↑ H. Eyal-Giladi, S. Kochav From cleavage to primitive streak formation: a complementary normal table and a new look at the first stages of the development of the chick. I. General morphology Dev. Biol., 49 (1976), pp. 321-337
- ↑ S. Kochav, M. Ginsburg, H. Eyal-Giladi From cleavage to primitive streak formation: a complementary normal table and a new look at the first stages of the development of the chick: II. Microscopic anatomy and cell population dynamics Dev. Biol., 79 (1980), pp. 296-308
- ↑ a b c O. Voiculescu, L. Bodenstein, I.J. Lau, C.D. Stern Local cell interactions and self-amplifying individual cell ingression drive amniote gastrulation eLife, 3 (2014)
- ↑ Weinberger, I. Brick Primary hypoblast development in the chick: II. The role of cell division Wilhelm Roux's archives of developmental biology, 191 (1982), pp. 127-133
- ↑ D.R. Canning, C.D. Stern Changes in the expression of the carbohydrate epitope HNK-1 associated with mesoderm induction in the chick embryo Development, 104 (1988), pp. 643-655.
- ↑ Y. Nakaya, E.W. Sukowati, Y. Wu, G.J. Sheng RhoA and microtubule dynamics control cell-basement membrane interaction in EMT during gastrulation Nat. Cell Biol., 10 (2008), pp. 765-775
- ↑ N. Yanagawa, M. Sakabe, H. Sakata, T. Yamagishi, Y. Nakajima Nodal signal is required for morphogenetic movements of epiblast layer in the pre-streak chick blastoderm Develop. Growth Differ., 53 (2011), pp. 366-377
- ↑ "http://worms.zoology.wisc.edu/frogs/gast/gast_morph.html"
- ↑ a b Peterson RE, McClay DR (2003). Primary mesenchyme cell patterning during the early stages following ingression.. Dev. Biol. 254 (1): 68–78. PMID 12606282. DOI: 10.1016/S0012-1606(02)00025-8.
- ↑ a b Gastrulation: Morphogenetic Movements.
- ↑ . http://biology.kenyon.edu/courses/biol114/Chap14/Chapter_14.html
- ↑ Shook DR, Keller R (2008). Epithelial type, ingression, blastopore architecture and the evolution of chordate mesoderm morphogenesis.. Journal of Experimental Zoology Part B: Molecular and Developmental Evolution 310 (1): 85–110. PMID 18041055. DOI: 10.1002/jez.b.21198.














