Tirozin
| Tirozin | |||
|---|---|---|---|
 | 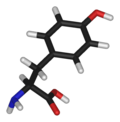 | ||
| IUPAC ime |
| ||
| Drugi nazivi | 2-Amino-3-(4-hidroksifenil)propanoinska kiselina | ||
| Identifikacija | |||
| Abrevijacija | Tyr, Y | ||
| CAS registarski broj | L) 60-18-4 (L) 60-18-4  Y Y | ||
| PubChem[1][2] | 1153 | ||
| MeSH | Tyrosine | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| Svojstva | |||
| Molekulska formula | C9H11NO3 | ||
| Molarna masa | 181.19 g mol−1 | ||
| Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
Tirozin je neurotransmiter i aminokiselina koja podstiče moždanu aktivnost. Najviše ga ima u mlečnim proizvodima, bananama, mahunama, avokadu, susamu i bademima.[3][4]
Tirozin (Tyr ili Y) pospešuje pravilan rad štitne žlezde, hipofize i tiroidne žlezde. Osim toga podstiče oslobađanje hormona rasta i proizvodi noradrenalin, koji smanjuje potrebu za jelom. Sprečava potištenost, umor i razdražljivost, pa je zbog toga pogodan i za zavisnike koji žele da se odviknu od kokaina.
Dopune L-tirozina je najbolje uzimati sa obrokom koji obiluje ugljenim hidratima ili pre odlaska na spavanje.
Reference
- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519. edit
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Darinka Koraćević, Gordana Bjelaković, Vidosava Đorđević. Biohemija. savremena administracija. ISBN 86-387-0622-7.
- ↑ David L. Nelson, Michael M. Cox (2005). Principles of Biochemistry (4th izd.). New York: W. H. Freeman. ISBN 0-7167-4339-6.
Literatura
- Donald Voet, Judith G. Voet (2005). Biochemistry (3 izd.). Wiley. ISBN 978-0-471-19350-0.
Spoljašnje veze
 | Portal Hemija |

- p
- r
- u

| |||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Opšte | |||||||||||||||||||||||
| N-terminus | |||||||||||||||||||||||
| C-terminus | |||||||||||||||||||||||
| Specifične aminokiseline |
| ||||||||||||||||||||||
B bsyn: dnk (repl, cycl, reco, repr) • tscr (fact, tcrg, nucl, rnat, rept, ptts) • tltn (risu, pttl, nexn) • dnab, rnab/runp • stru (domn, 1°, 2°, 3°, 4°) | |||||||||||||||||||||||
| |
|---|---|
| Sekundarna struktura proteina | Heliksi: α-heliks • 310 heliks • π-heliks • β-heliks • Poliprolinski heliks • Kolagenski heliks Ispružena: β-ravan • Okret • Beta ukosnica • Beta izbočina • α-ravan Supersekundarna: Upredena zavojnica • Heliks-okret-heliks • EF ruka |
| Aminokiseline | Favorizuju heliks: Metionin • Alanin • Leucin • Glutaminska kiselina • Glutamin • Lizin Favorizuju izdužene strukture: Treonin • Izoleucin • Valin • Fenilalanin • Tirozin • Triptofan Favorizuju neuređene strukture: Glicin • Serin • Prolin • Asparagin • Asparaginska kiselina Bez preferencije: Cistein • Histidin • Arginin |
| |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||
| |||||||||||||||||||||
| |||||||||||||||||||||
| |||||||||||||||||||||
| |||||||||||||||||||||
| |||||||||||||||||||||
 | Ovaj članak o biologiji je u začetku. Možete pomoći Wikipediji tako što ćete ga proširiti. |





